Autorizzato nel Regno Unito il primo studio clinico sulla terapia di rimielinizzazione PTD802
Il candidato di Pheno Therapeutics è un inibitore del recettore GPR17
La Medicines and Healthcare products Regulatory Agency (MHRA) del Regno Unito ha autorizzato Pheno Therapeutics ad avviare la prima sperimentazione clinica di fase 1 sull’uomo per testare il suo candidato orale PTD802 su volontari sani.
La terapia è un antagonista selettivo di piccole molecole, o inibitore, del recettore GPR17 ed è progettata per ripristinare la mielina danneggiata e persa , un processo noto come rimielinizzazione, nelle persone affette da sclerosi multipla (SM) e potenzialmente da altre condizioni demielinizzanti.
“Siamo lieti di aver ricevuto l’approvazione dalla MHRA per far progredire il nostro programma PTD802 verso una sperimentazione di Fase 1, una pietra miliare importante, che segna la nostra transizione verso un’organizzazione in fase clinica. Come prima azienda a effettuare il dosaggio di un antagonista selettivo del GPR17 in esseri umani sani, stiamo aprendo la strada alla corsa per sviluppare terapie di rimielinizzazione mirate al GPR17”, ha affermato Fraser Murray, PhD, CEO di Pheno Therapeutics, in un comunicato stampa aziendale . “Con questo programma first-in-human ci stiamo avvicinando al nostro obiettivo di fornire farmaci trasformativi per il trattamento di malattie neurologiche associate alla demielinizzazione”.
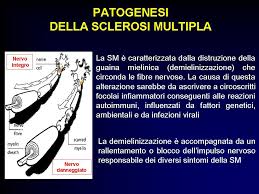
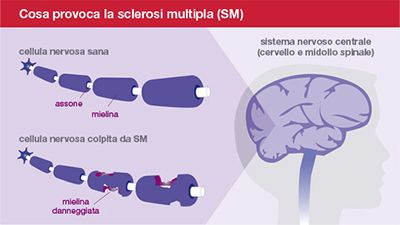
La SM è causata dal sistema immunitario che prende erroneamente di mira la mielina, uno strato protettivo che circonda le fibre nervose ed è importante per la trasmissione efficiente dei segnali nervosi. Quando la mielina viene persa, anche le cellule nervose vengono danneggiate e i pazienti sperimentano una serie di sintomi correlati alla segnalazione nervosa compromessa.
Un “bisogno urgente” di terapie di rimielinizzazione
La ricerca di terapie che promuovano la riparazione della mielina è stata un obiettivo chiave nella ricerca sulla SM per molti anni. Esistono diversi trattamenti che riducono l’infiammazione e prevengono o rallentano ulteriori danni, ma nessuno può invertire il danno che si è già verificato.
“Gli attuali trattamenti per la SM si concentrano principalmente sugli aspetti immunitari della malattia, riducendo la gravità e la frequenza delle ricadute. C’è un bisogno urgente e insoddisfatto di terapie efficaci che limitino la progressione della disabilità nella SM, con la rimielinizzazione che offre un promettente trattamento neuroprotettivo”, ha affermato Siddharthan Chandran, MD, PhD, co-fondatore di Pheno Therapeutics.
Il recettore GPR17 funziona come un freno naturale che rallenta lo sviluppo degli oligodendrociti, le cellule che producono mielina nel cervello e nel midollo spinale. PTD802 è progettato per aumentare la rimielinizzazione rilasciando questo freno. Pheno ritiene che possa essere utilizzato con le terapie SM esistenti per controllare meglio la progressione della malattia e possibilmente aiutare i pazienti a recuperare alcune funzioni perdute.
“Sebbene gli antagonisti del GPR17 abbiano una potenziale utilità oltre la SM, PTD802 è un agente di rimielinizzazione orale di prima categoria estremamente promettente, che crediamo sarà il prossimo passo nell’ideazione di approcci combinatori per prevenire la progressione della SM”, ha affermato Chandran.
Patricia Inacio, PhD Patricia ha conseguito il dottorato di ricerca in biologia cellulare presso l’Università Nova de Lisboa, Portogallo, ed è stata autrice di diversi progetti di ricerca e borse di studio, nonché di importanti domande di sovvenzione per agenzie europee. Ha anche lavorato come assistente di ricerca studentesca di dottorato presso il Dipartimento di Microbiologia e Immunologia, Columbia University, New York, per il quale le è stata assegnata una borsa di studio della Luso-American Development Foundation (FLAD).
PIPE 307
Contineum Therapeutics, Inc. Completa l’arruolamento nello studio di Fase 2 PIPE-307 per il trattamento della Sclerosi Multipla Recidivante-Remittente (SMRR)
08 gennaio 2025
STUDIO VISTA
Contineum Therapeutics, Inc. ha annunciato di aver completato l’arruolamento mirato di 168 pazienti nello studio di Fase 2 PIPE-307 VISTA. PIPE-307 è un antagonista del recettore M1 potenzialmente primo della classe, in fase di sviluppo per i pazienti con sclerosi multipla recidivante-remittente (SMRR). Cioè bloccando questo recettore, si vengono a generare oligodendrociti che sviluppano la mielina. Lo studio di Fase 2, randomizzato, in doppio cieco, controllato con placebo, multicentrico, di PIPE-307 valuterà la sicurezza e l’efficacia nei pazienti con SMRR.
Lo studio è progettato per misurare più endpoint clinici (esiti dello studio)e di imaging sensibili ai cambiamenti nella rimielinizzazione nella SMRR. Contineum prevede che l’ultimo paziente completerà lo studio PIPE-307 VISTA nel terzo trimestre del 2025. PIPE-307 viene sviluppato in base a un accordo di licenza e sviluppo globale tra Contineum e Janssen Pharmaceutica NV, una società di Johnson & Johnson.
Questo nuovo farmaco agisce su un recettore specifico, chiamato M1R, presente su alcune cellule cerebrali. Bloccando questo recettore, PIPE-307 stimola la maturazione degli oligodendrociti, le cellule responsabili della produzione di mielina. È come se il farmaco desse il via libera a un esercito di “riparatori”, pronti a ricostruire l’isolamento perduto intorno ai neuroni danneggiati
